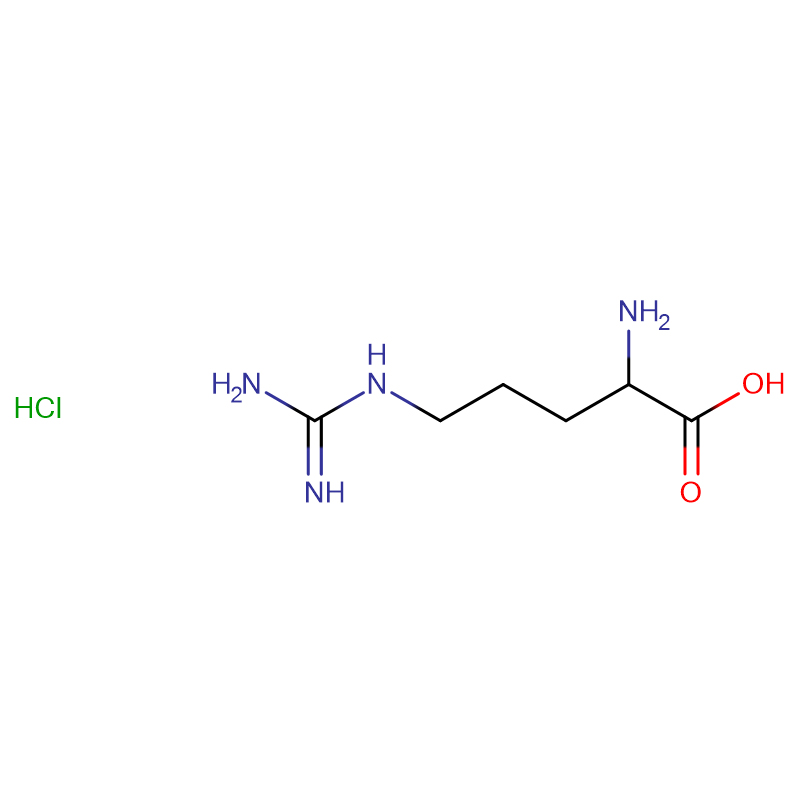
L-Arginin CAS: 74-79-3 99% Ağ kristallar və ya kristal toz
| Kataloq nömrəsi | XD90323 |
| Məhsulun adı | L-arginin |
| CAS | 74-79-3 |
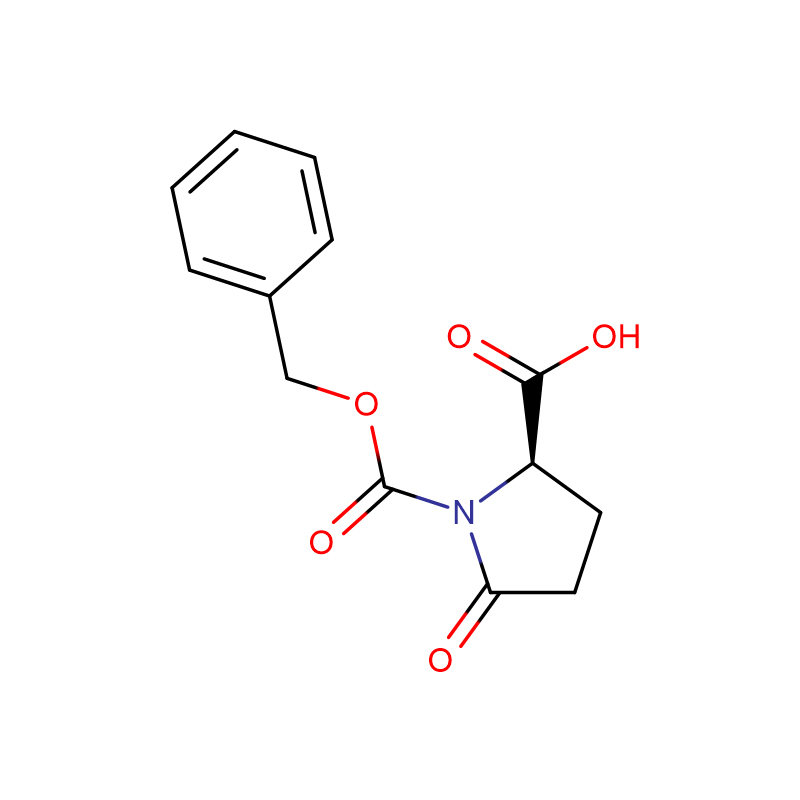
| Molekulyar Formula | C6H14N4O2 |
| Molekulyar çəki | 174.20 |
| Saxlama Detalları | Ətraf mühit |
| Uyğunlaşdırılmış Tarif Məcəlləsi | 29252900 |
Məhsulun spesifikasiyası
| Görünüş | Ağ kristallar və ya kristal toz |
| Təhlil | 99% |
| İdentifikasiya | İnfraqırmızı udma |
| Qurutma zamanı itki | ≤ 0,5% |
| Xromatoqrafik təmizlik | Hər hansı fərdi çirklərin 0,5%-dən çoxu aşkar edilmir; Ümumi çirklərin 2,0%-dən çoxu aşkar edilmir. |
| Alovlanma zamanı qalıq | ≤ 0,3% |
| Ağır metallar (PB) | ≤ 0,0015% |
| Dəmir (Fe kimi) | ≤ 0,003% |
| Sulfat (SO4 kimi) | ≤ 0,03% |
| Usp dərəcəsi | USP 33 |
| Xlorid (CI) | ≤ 0,05% |
| Xüsusi fırlanma [ α ] D 2 5 | +26,3 ° ~ +27,7 ° |
Flavindən asılı l-lizin monooksigenaza olan Mycobacterium smegmatis G (MbsG) mexanizmi ilkin və həlledici kinetik izotop effektləri, substratın analoqları, pH və həlledicinin özlülüyünün təsirindən mexaniki zondlar kimi istifadə edilməklə, stabil vəziyyət və sürətli reaksiya şəraitində tədqiq edilmişdir.Nəticələr göstərir ki, l-lizin NAD(P)H-dən əvvəl bağlanır ki, bu da flavin reduksiyası üçün sürət sabitinin azalmasına gətirib çıxarır.l-lizin bağlanması, C4a-hidroperoksiflavin ara məhsulunun müşahidəsi olmadan bir addımlı prosesdə baş verən flavin oksidləşmə sürətinə təsir göstərmir.Oxşar təsirlər bir neçə substrat analoqları ilə müəyyən edilmişdir.Flavinin oksidləşməsi pH-dan asılı deyil, NAD(P)H üçün kcat/Km və kred/KD pH profilləri pH azaldıqca aktivliyin artması ilə ~6.0 vahid pKa dəyərləri nümayiş etdirir.Aşağı pH-da ferment daha çox ayrılır, daha çox hidrogen peroksid və superoksid əmələ gətirir.Hidrid ötürülməsi neytral pH-da sürəti qismən məhdudlaşdırır və aşağı pH-da sürəti daha çox məhdudlaşdırır.Neytral pH-da NAD(P)H üçün kcat/Km-ə tərs həlledici özlülük təsiri, aşağı pH-da isə normal həlledici özlülük effekti müşahidə edilmişdir.Nəticələr birlikdə, lizinin hidroksilləşməsinin səmərəliliyinə təsir edən reduktiv yarım reaksiyada sürəti məhdudlaşdıran və pH-həssas konformasiya dəyişikliyinin baş verdiyi unikal mexanizmi göstərir.